
Последние годы слово “эпигенетика” все чаще встречается в статьях, посвященных различным сферам медицины. Эпигенетике посвящаются конференции, в т.ч. и в России. И для того, чтобы не ударить в грязь лицом, пытаясь поддержать очередную светскую беседу, оказавшись на таком мероприятии, мы решили, что пора наконец разобраться, что же это такое.
Эпигенетика – область генетики, исследующая принципы наследования и процессы изменения экспрессии генов или фенотипа клетки, вызванных механизмами, не затрагивающими последовательности ДНК. Для того чтобы понять это, стоит лишь представить перед собой текст (Рис. 1). В нетронутом виде, при хорошем зрении и освещении мы способны увидеть любой из его фрагментов, а при желании даже прочесть целиком. Однако, если пролить на него чернила, определенная часть текста будет недоступна для считывания и картина, которую мы представим, прочитав оставшийся фрагмент может разительно отличаться от той, что предстает перед нами при прочтении полной версии.

Рис. 1 Экспрессия портала “Психиатрия & Нейронауки”
Примерно таким образом работают различные эпигенетические механизмы. Среди них можно выделить основные процессы:
- Метилирование ДНК;
- Модификация гистонов (метилирование, фосфорилирование, убиквитинирование и рибозилирование). Эти процессы могут контролировать экспрессию белка, поддерживать структуру хроматина, инактивировать Х-хромосому. Последний механизм связан с гендерными различиями в проявлениях многих нозологий (подробнее: Вклад нейроиммунологии и нейроэпигенетики в формирование половых различий мозга);
- Ремоделирование хроматина. Хроматин не однороден по своей структуре. Он выступает в различных формах упаковки – от фибриллы высококонденсированного хроматина (известного как гетерохроматин) до менее компактизированной формы, где гены обычно экспрессируются (известной как эухроматин);
- Прионные механизмы, известные всем по ужасным заболеваниям, которые они вызывают (куру, фатальная семейная бессонница и т.д.). Эти механизмы связаны с тем что прионные белки обладают аномальной трёхмерной структурой и способны катализировать структурное превращение гомологичных им нормальных белков в себе подобный (прионный) белок, присоединяясь к белку-мишени и изменяя его конформацию;
- Системы структурной наследственности;
- МикроРНК: некодирующие небольшие отрезки РНК, которые могут изменять стабильность и трансляцию мРНК. Ученые признают роль микроРНК в дендритогенезе, формировании памяти. У пациентов с шизофренией обнаруживалось изменение в экспрессии микроРНК.
Результаты этих влияний могут быть разными. Это активация определенных генов и ингибирование других, а также регуляция уровня экспрессии того или иного гена.
Самым изученным эпигенетическим механизмом является метилирование ДНК. Метилирование ДНК заключается в присоединении метильной группы к цитозину. Если этот процесс происходит в промоторной зоне гена, то это, как правило, приводит к супрессии соответствующего гена. Метилированный цитозин может затем окисляться особыми ферментами, что в конечном итоге приводит к его деметилированию обратно в цитозин, после чего ген вновь может свободно экспрессироваться (Рис. 2).
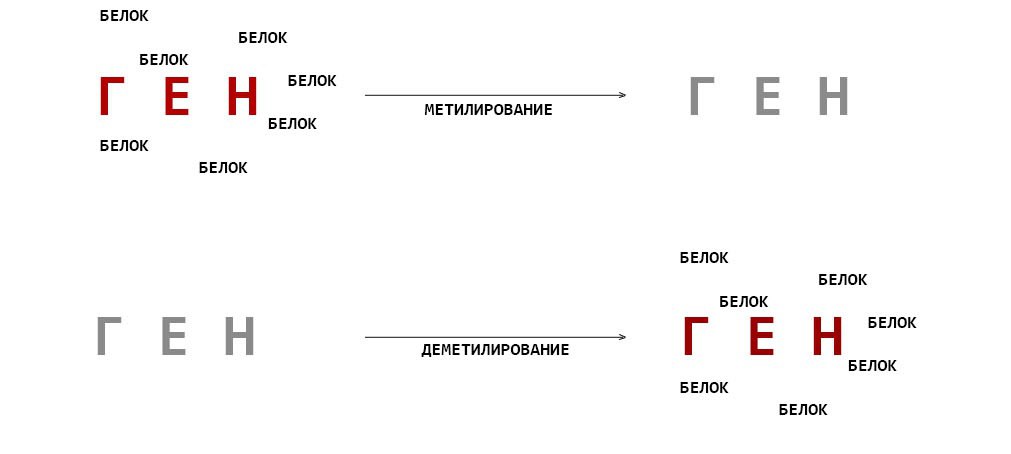
Рис. 2 Эффект метилирования ДНК
Этот механизм наблюдался в серии клинических испытаний, проведенных в конце 1960-х годов с целью поиска лучшей терапии для больных шизофренией (Parketal., 1965; Antunetal., 1971; обзор в работе Costaetal., 2002). Основанием для проведения экспериментов послужил следующий довод: галоперидол блокирует дофаминовые рецепторы, следовательно, если в головном мозге произойдет снижение дофамина, стоит ожидать улучшения состояния. Для этого больным шизофренией и контрольной группе давали в большом количестве метионин, который повышает уровень ферментов метаболизирующих дофамин посредством его метилирования. Однако вместо ожидаемого улучшения пациенты демонстрировали обострение симптоматики. Первым предположением было то, что метионин индуцировал синтез одного из метаболитов дофамина, способного вызвать психотический эпизод. Однако уровни различных метаболитов оставались неизменными. Механизм метионин-обусловленного рецидива психотических симптомов на самом деле был связан с изменением экспрессии определенных генов, в частности гена белка рилина, колебания уровня которого коррелируют с выраженностью психотических проявлений при шизофрении и биполярном расстройстве. Позже был изучен интересный факт. Некоторые лекарства (такие как вальпроевая кислота, клозапин, сульпирид) помимо своих рецепторных влияний, также действуют и на эпигенетические механизмы, приводя к деметилированию ДНК, а соответственно к активации экспрессии гена, что является дополнительным путем воздействия на продуктивную симптоматику.Вышеупомянутые процессы метилирования причастны также к механизмам формирования долговременной памяти.
Одним из самых важных и интересных моментов являются пути воздействия на эпигенетические механизмы, потому как здесь эпигенетика делает попытки примирить двух самых заклятых врагов: генетические и средовые факторы. Как показал описанный выше опыт, на работу генетического материала можно воздействовать извне, и это могут быть не только химические вещества, влияния оказывают также и психосоциальные факторы: экстремальные ситуации, обучение, психотерапия. Однако диапазон в котором эти внешние влияния будут работать все же зависит от генетической предрасположенности.
Так, в исследованиях на грызунах было обнаружено, что постоянное воздействие нескольких форм стрессовых факторов вызывает изменение структуры хроматина в головном мозге. Один вид модификаций отмечался во всех случаях: хронический стресс вызывает изменение общего клеточного уровня ацетилированных или метилированных гистонов в определенных участках лимбической области головного мозга. Эти выявляемые во всех случаях изменения, возможно, отражают общегеномный сдвиг в сторону усиления или, наоборот, ограничения уровня активности хроматина. Другой тип модификаций является характерным для определенных локусов и представляет собой изменение в ацетилировании или метилировании гистонов или в метилировании ДНК, происходящее на уровне определенного гена, опосредованное изменением его экспрессии. Интересно, что многие из этих специфических для локусов изменений являются препятствием для случайных глобальных модификаций.
Подобная эпигенетическая регуляция стрессовых реакций проиллюстрирована в одной из работ, посвященной депрессии. При хроническом социальном стрессе у мышей с повышенной восприимчивостью манифестировал депрессивноподобный синдром, в то время как у мышей с нормальной восприимчивостью симптоматика заболевания не развивалась, несмотря на подверженность тому же уровню стресса. Было доказано, что подобный уровень восприимчивости частично регулируется изменениями в гистонномацетилировании и деметилировании в центре удовольствия.
При повышении общего уровня ацетилирования гистонов, обеспечивается устойчивость к стрессу, снижает восприимчивость к социальным факторам и вызывает реакцию, сходную с действием антидепрессантов. Деметилирование в этом случае, напротив, обладает патологическим действием.
Существуют веские доказательства значимости эпигенетических модификаций, происходящих на раннем периоде жизни и вызывающих повышенную чувствительность к стрессу в течение всей жизни. Эксперименты на крысах показали, что у мышат, выросших в условиях недостатка материнской заботы, был обнаружен повышенный уровень реакции на стресс, а также повышенный уровень тревожности во взрослом возрасте по сравнению с грызунами, получавшими материнский уход в достаточном количестве.
Традиционно для каждого текста хоть как-то связанного с биологической психиатрией мы просто обязаны упомянуть Амигдалу, тем более что она этого заслуживает. Амигдала является центром обработки информации из окружающей среды и трансформирования ее в воспоминания с помощью молекулярных механизмов. Двумя важными аспектами этого процесса является обработка устрашающих сигналов и стимулов вознаграждения: амигдала помнит, чего нужно бояться а к чему стремиться, и поэтому играет важную роль в развитии тревожных расстройств и расстройств, связанных с злоупотреблением психоактивными веществами. Животные модели предполагают, что, как только формируются реакции страха или вознаграждения, образуются и новые синапсы, связанные с этими реакциями, существование которых становится постоянным и необратимым. Во время восстановления после таких событий с помощью процессов обучения, описанные связи не теряются, однако появляются новые синапсы, которые блокируют работу первых. Это требует долгосрочного потенцирования NMDA-рецепторов, а также включения определенных эпигенетических механизмов ответственных за дендритообразование. Психотерапия и психофармакотерапия воздействуя на эти мишени могут способствовать формированию этих новых синапсов, которые блокируют воспоминания о страхе или награде. Вот очевидное объяснение не только того, как психотерапия может гипотетически изменять симптомы, изменяя схемы нейронов, но также и то, как сочетание лекарств, которые способствуют нейротрансмиссии NMDA, потенциально может повысить эффективность психотерапии и таким образом ускорить выздоровление.
В настоящее время психотерапия может быть концептуализирована не только ее классическими психодинамическими принципами, но и как нейробиологический зонд, способный индуцировать эпигенетические изменения в схемах головного мозга, мало чем отличающийся от конечных действий психотропных препаратов. Оценка эпигенетических изменений в мозге живого человека вряд ли будет возможна в ближайшее время, однако возможна оценка периферических клеток, таких как лимфоциты, для того чтобы уже сейчас на объективном уровне оценивать результаты психотерапевтических воздействий.
Пдготовила: Чеснокова О.И.
Литература:
1 – Stahl S. M. Psychotherapy as an epigenetic ‘drug’: psychiatric therapeutics target symptoms linked to malfunctioning brain circuits with psychotherapy as well as with drugs //Journal of clinical pharmacy and therapeutics. – 2012. – Т. 37. – №. 3. – С. 249-253.
2 – Peedicayil J. Role of epigenetics in pharmacotherapy, psychotherapy and nutritional management of mental disorders //Journal of clinical pharmacy and therapeutics. – 2012. – Т. 37. – №. 5. – С. 499-501.
3 – Tsankova N. et al. Epigenetic regulation in psychiatric disorders //Nature reviews.Neuroscience. – 2007. – Т. 8. – №. 5. – С. 355.
4 – Nestler E. J. et al. Neurobiology of depression //Neuron. – 2002. – Т. 34. – №. 1. – С. 13-25.
5 – Нестерович А. Н. Эпигенетические аспекты этиопатогенеза шизофрении //Медицинские новости. – 2012. – №. 10.
6 – Чуриков Н. А. Молекулярные механизмы эпигенетики (обзор) //Биохимия. – 2005. – Т. 70. – №. 4. – С. 493-513.
7 – Costa E. et al. REELIN and Schizophrenia //Molecular interventions. – 2002. – Т. 2. – №. 1. – С. 47.