
О положительном дексаметазоновом тесте у пациентов с меланхолической депрессией, свидетельствующем о гиперактивации гипоталамо-гипофизарно-надпочечниковой оси (ГГН-оси), известно ещё со студенческой скамьи. Более того, гиперактивация ГГН-оси является мощным биологическим коррелятом депрессии наряду с дисфункцией моноаминовых нейромедиаторных систем и считается одним из основных звеньев её патогенеза. Однако за последние несколько десятилетий знания учёных о том, как функционирует ГГН-ось значительно расширились. Теперь стало понятно, что помимо функционирования гипоталамуса, гипофиза и надпочечников, занимающих одно из центральных мест в патогенезе депрессии, в патологический процесс вовлечено куда большее количество областей головного мозга и его нейромедиаторных, а также нейропептидных систем. Такое «расширение» теории гиперактивации ГГН-оси при депрессии позволяет по-новому взглянуть на механизмы развития данного расстройства, а также найти новые специфические мишени для лекарственной терапии. Также стоит отметить, что гиперактивация ГГН-оси встречается только у 70% пациентов с данным расстройством, и не характерна для таких типов депрессии, как климактерическая, атипичная или сезонная, для которых свойственно, наоборот, уменьшение активности ГГН-оси.
Рис. 1 Функционирование ГГН-оси в норме
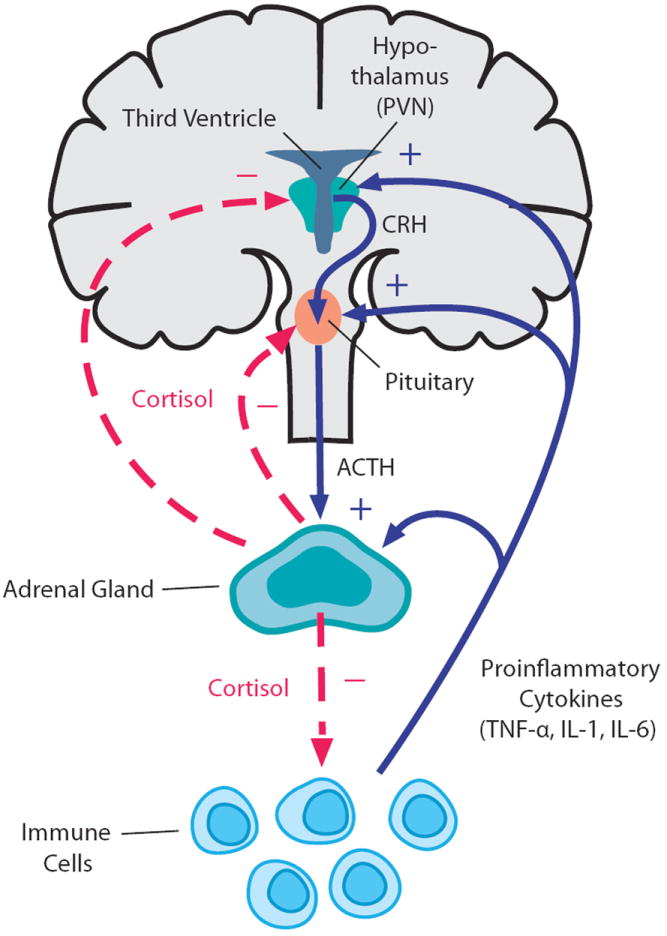
Стимул, вызвавший стрессор, достигает ГГН-ось из миндалевидного тела. В ответ на это в паравентрикулярном ядре гипоталамуса высвобождается вазопрессин и кортикотропин-рилизинг гормон (КРГ) – главный регулятором ГГН-оси. Он состоит из 41 аминокислотного остатка, а его синтез регулируется геном CRF. Вместе с вазопрессином КРГ по системе портальных вен попадает в передние доли гипофиза и стимулирует продукцию прогормона проопиомеланокортина (ПОМК), который затем перерабатывается в аденокортикотропный гормон (АКТГ), опиоиды и меланокортин. АКТГ, в свою очередь, стимулирует высвобождение в пучковой зоне коркового вещества надпочечников глюкокортикоидов (кортизола у людей и кортикостерона у мышей), которые в дальнейшем оказывают отрицательную обратную связь на гипофиз и гипоталамус посредством воздействия на минералкортикоидные (МР) и глюкокортикоидные рецепторы (ГР), из-за чего уменьшается степень активации ГГН-оси (Marni N. Silverman, 2012).
Несмотря на распространённое мнение, что главные проявления гиперактивации ГГН-оси связаны только лишь с гиперкортизолемией, появляется всё больше данных, что повышенный уровень кортикотропин-рилизинг гормона (КРГ), являющимся главным регулятором ГГН-оси, обладает, куда большим негативным эффектом на функциональные системы головного мозга.
Эффекты, проявляемые КРГ, зависят от зон его синтеза и мест наибольшей концентрации его рецепторов. Так, помимо гипоталамуса, он выделяется также в нейронах миндалевидного тела, гиппокампа и голубого пятна. Данный нейропептид оказывает локальное нейромодулирующие воздействие на нейроны в течение нескольких секунд после высвобождения, действуя через два специфических рецептора КРГ 1 и 2 типов (КРГР1, КРГР2), которые широко распространены в различных отделах головного мозга. Стоит также отметить, что к семейству КРГ-нейропептидов, помимо самого КРГ, относятся ещё и урокортины (UCN 1, 2 3), которые также как и возопрессин, орексин и динорфин влияют на гомеостаз мозга.
В зависимости от дозы и времени воздействия КРГ на мишени различаются и его эффекты. Например, высвобождение КРГ в оптимальных дозах при остром стрессе в центральном ядре миндалевидного тела способствуют консолидации памяти, а в гиппокампе – увеличению пластичности синапсов. Однако при воздействии высоких доз КРГ в течение длительного времени происходит ухудшение функции гиппокампа, что проявляется повреждением нейронов и уменьшением числа синапсов.
Так, в течение всего эпизода меланхоличной депрессии у пациентов обнаруживается повышенный уровень КРГ в плазме и церебро-спинальной жидкости. В патологоанатомических исследованиях умерших людей, страдавших депрессией, найдены доказательства гиперактивности КРГ в паравентрикулярных ядрах гипоталамуса, корковых областях, ядрах моста и голубом пятне. В то же время, повышенный уровень КРГ у лиц с депрессией снижался после курса электросудорожной или антидепрессивной терапии.
Более того, у здоровых индивидов, в семьях которых высок генетический риск развития депрессии, результаты комбинированного ДЕКС/КРГ теста (DEX/CRH: dexamethasone-suppression/corticotropin-releasinghormone-stimulationtest), который сочетает супрессию дексаметазоном со стимуляцией КРГ, оказываются в промежутке между результатами пациентов с депрессией и контрольной группой здоровых добровольцев. Данные результаты указывают на то, что даже небольшие изменения в функционировании ГГН-оси имеют генетический бэкграунд, который с возрастом повышает риск развития депрессии или других опосредованных стрессом заболеваний. В другом исследовании показано, что у лиц с депрессией значительно повышена частота G-аллеля полиморфизма (rs242939) гена КРГР1 в сравнении с контрольной группой. В совокупности, эти наблюдения поддерживают концепцию того, что дисрегуляция ГГН-оси, которая проявляется в том числе повышенным уровнем КРГ, возможно, связана с генетической предрасположенностью и представляет фактор риска развития депрессии.
При депрессии также наблюдается снижение активности нейротрофических факторов. Это приводит к снижению синаптических связей в гиппокампе и префронтальной коре, что коррелирует с депрессивной симптоматикой. Обнаружено наличие тесной связи между нейротрофическими факторами, в частности нейротрофическим фактором мозга (BDNF), и КРГ, который модулирует их продукцию, выработку и активность.
Интересно и то, что изменения в рецепторном аппарате КРГ так же влияют на формирование определенных симптомокомплексов. Так, повторные воздействия стресса приводят к изменение соотношения КРГР1 и КРГР2 в сторону увеличения КРГР1в областях, связанных с депрессией. КРГР1 способен модулировать тревожное поведение и независимо от ГГН-оси, а его недостаток защищает человека от формирования негативных последствий стресса не зависимо от возраста. Это связано с тем, что КРГР1 контролируют глутаматергические, норадренолинергические и дофаминергические нейронные контуры, внося значимый вклад в проявления расстройств, связанных со стрессом.
Это подтверждают и обширные данные, свидетельствующие о том, что три основные нейромедиаторные системы (серотониновая, норадренолиновая и дофаминовая) тесно взаимодействуют и влияют на уровнь КРГ. Так, в голубом пятне (важнейшее ядро норадреналинергической системы в головном мозге), дорсальных ядрах шва (важнейшее ядро серотонинергической системы) и в вентральной области покрышки (важнейшее ядро мезокортиколимбической дофаминергической системы) обнаруживается высокий уровень экспрессии КРГР1 и КРГР2, а общий уровень экспрессии этих рецепторов и их соотношение – важный показатель индивидуальной переносимости стресса и риска развития депрессии.
Например, в дорсальном ядре шва КРГ имеет противоположные эффекты на серотонинергическую систему в зависимости от того на какие рецепторы (КРГР1 или КРГР2) он действует. Так, активация КРГР1 в этой области приводит к усилению ГАМК-ергических тормозящих воздействий на серотониновую систему, а активация КРГР2 оказывает, наоборот, потенцирующие действие.
Также доказано влияние КРГ на формирование ангедонии, которая характеризуется снижением активности в мезолимбических дофаминовых проекциях от вентральной области покрышки до прилежащего ядра (вентральный стриатум) и далее до коры головного мозг. КРГ в период острого стресса стимулирует выброс дофамина в прилежащем ядре, что является важным звеном системы «вознаграждения». Однако, после сильного острого стресса или при его длительном воздействии, КРГ не стимулирует выброс дофамина, что можно рассматривать как один из механизмов формирования ангедонии.
Дисбаланс в нейромедиаторных системах затрагивает и саму ГГН-ось, так как ацетилхолин, дофамин и норадреналин содействуют секреции КРГ в гипоталамусе, а серотонин, в свою очередь, ингибирует секрецию КРГ в гипоталамусе и АКТГ в гипофизе, что тоже вносит свой вклад в дисфункцию ГГН-оси.
Ещё одна важная особенность физиологии депрессии заключается в растормаживании REM-фазы сна (REM, Rapid Eye Movement с англ. «быстрое движение глаз»), которое специфично связывают с центральной активностью КРГ и снижением уровня соматотропин-рилизинг-гормона (СРГ), регулирующего медленноволновой сон. Так, в одном клиническом исследовании по оценке безопасности и переносимости антагонистов КРГР1 (R121919) проводились записи ЭЭГ во время сна до и после 28 дней лечения. По результатам оказалось, что большинство пациентов со значительными нарушениями REM-стадии сна показали улучшение симптомов депрессии между 50 и 90% по шкале Гамильтона для оценки депрессии, в то время как улучшение у пациентов с нормальными стадиями сна было стабильно ниже 50%.
Рис. 2 Нарушение сна при депрессии

Нарушение сна при депрессии характеризуется нарушением медленно-волнового сна и увеличением REM-фазы сна в результате дисбаланса между КРГ и СРГ (Steiger, 2003).
Обобщённые результаты позволяют предположить, что растормаживание REM-фазы сна вероятно, может рассматриваться как специфический показатель, отражающий центральную активность КРГ, с помощью которого возможно выделение пациентов с депрессией, у которых целесообразно проведение терапии антагонистами КРГР1, широко использующихся для терапии эндокринологических заболеваний.
Источник: Касьянов Е.Д., Мазо Г.Э. Функционирование гипоталамо-гипофизарно-надпочечниковой оси при депрессии: актуальное состояние проблемы. // Журнал Психическое здоровье. – 2017. – №8. – С. 27 – 34.
Добавить комментарий